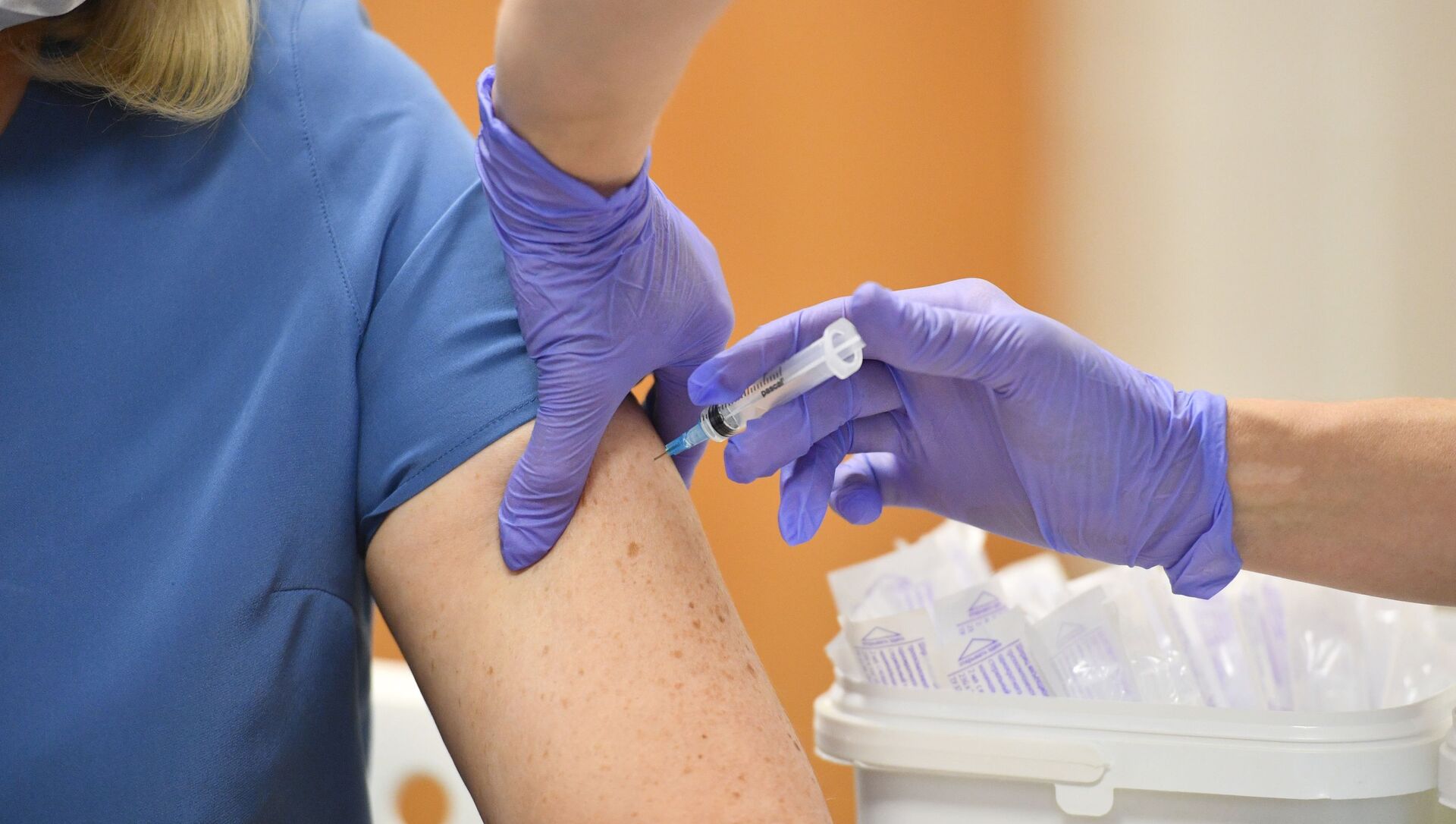
欧州医薬品庁の医薬品委員会は、中国のSinovac Life Sciencesが開発を行った新型コロナウイルス用不活性化ワクチンVero Cellの逐次審査のプロセスを開始したと発表した。
評定開始の決定は前臨床データおよび臨床実験に基づくもので、これらの実験によりワクチンが新型コロナウイルスの原因となるSARS-CoV-2に対する抗体を作り、感染症から人体を保護し得ると推測されている。
発表によれば、EMAはワクチンの優位性がリスクの可能性を上回るかどうかを解明する予定だという。逐次審査は、欧州におけるワクチン接種承認に向けた公的申請証明に必要となる十分な基礎データを得るまで継続されることになる。
逐次審査とは、EMAが公衆衛生分野の非常事態時に効果が期待される製薬の評価を促進する手法のこと。現在、手続きは他にもロシア製ワクチン「スプートニクV」とキュアバック社の「CVnCoV」、ノババックス社の「Novavax」の3種類のワクチンに関しても行なわれている。